
Fda conferma l'efficacia di Pfizer, i risultati di Moderna
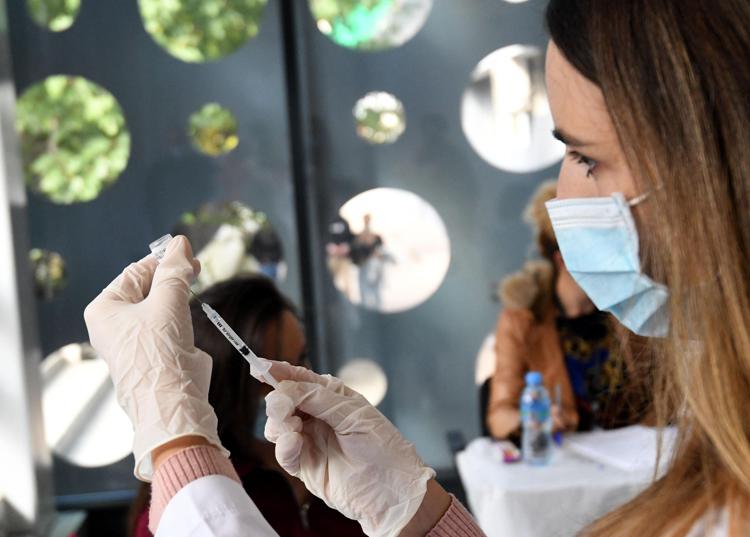
Vaccino anti-covid Pfizer e Moderna nella fascia 5-11 anni. E' efficace? Qual è il 'bugiardino'? Come funziona il vaccino con prima e seconda dose? A definire il quadro, anche per effetti e sintomi, sono soprattutto news da Moderna e Pfizer. "Non vi sono dubbi su come la vaccinazione in età pediatrica sarà l'indispensabile completamento della campagna vaccinale" contro Covid-19. "Proteggerà direttamente adulti e bambini", afferma Guido Rasi, ex direttore esecutivo dell'Agenzia europea del farmaco Ema, direttore scientifico di Consulcesi e consulente del commissario Figliuolo in tema vaccini, provando a fare chiarezza sull'opportunità di immunizzare o meno i bambini.
"Non ci sono timori per il vaccino ai bambini tra 5 e 12 anni", ha spiegato dal canto suo Franco Locatelli, presidente del Consiglio superiore di Sanità e coordinatore del Comitato tecnico scientifico.
Il vaccino anti-Covid di Pfizer/BioNTech ha avuto un tasso di efficacia del 90,7% nella prevenzione dell'infezione sintomatica fra i bimbi dai 5 agli 11 anni, secondo i dati di uno studio clinico che l'americana Pfizer ha presentato all'Agenzia del farmaco Fda di cui è atteso il responso. La notizia rimbalza sui media statunitensi. I bambini under 12 coinvolti nel trial hanno ricevuto una dose di 10 microgrammi, inferiore di un terzo rispetto a quella somministrata alle popolazioni di età superiore (30 microgrammi). Secondo i risultati sottoposti dai produttori alla Fda, il dosaggio si è dimostrato sicuro e gli effetti collaterali riportati erano lievi. Dei 2.268 bimbi reclutati, ha ricevuto il vaccino una quota doppia rispetto al gruppo placebo. Nel gruppo controllo hanno contratto Covid 16 bambini, mentre tra i vaccinati se ne sono ammalati 3: un'efficacia superiore al 90%.
Pfizer ha sottoposto i primi dati in vista di un incontro in programma la prossima settimana, in cui il comitato consultivo della Fda deciderà se raccomandare all'agenzia di concedere l'autorizzazione a Comirnaty nella fascia under 12. Se la Fda dirà sì, la palla passerà ai Centers for Disease Control and Prevention (Cdc) che il mese prossimo forniranno le indicazioni operative per la campagna nei bimbi.
Nei bambini da 6 a 11 anni il vaccino anti-Covid di Moderna "mostra una robusta risposta immunitaria" e un "profilo di sicurezza favorevole". Gli effetti indesiderati sono stati "di gravità lieve o moderata", i sintomi "più comuni sono stati affaticamento, cefalea, febbre e dolore al sito di iniezione". Ad annunciarlo è stata l'azienda Usa, presentando i primi dati di uno studio di fase 2/3 condotto in questa fascia d'età. Dati "positivi", spiega la società in una nota. Nel trial sono state valutate due dosi da 50 microgrammi del vaccino mRna-1273. Queste sono state "generalmente ben tollerate e hanno mostrato titoli di anticorpi neutralizzanti robusti".
Moderna spiega che gli endpoint primari, gli obiettivi di immunogenicità, sono stati raggiunti e prevede di presentare "presto, nel breve termine", i risultati alla statunitense Fda, all'Agenzia europea del farmaco Ema e ad altre agenzie regolatorie nel mondo.
L'analisi ad interim mostra i risultati dello studio KidCove nei bambini di età compresa tra 6 e meno di 12 anni dopo le due dosi di 50 µg. In questa coorte sono stati arruolati 4.753 partecipanti di questa fascia d'età. Nello studio, il rapporto delle medie geometriche (Gmr) dei titoli di anticorpi neutralizzanti anti Sars-CoV-2, che confrontava la risposta nei bambini con la risposta nei giovani adulti dello studio Cove di fase 3, era 1,5, con un tasso di sierorisposta del 99,3%. Questi risultati, argomenta Moderna, "dimostrano una forte risposta immunitaria in questa coorte di bambini un mese dopo la seconda dose".
"Siamo incoraggiati dall'immunogenicità e dal profilo di sicurezza dell'mRna-1273 nei bambini di età compresa tra 6 e meno di 12 anni", dichiara il Ceo di Moderna, Stéphane Bancel. "Non vediamo l'ora di presentare richiesta" di approvazione "alle autorità regolatorie a livello globale e rimaniamo impegnati a fare la nostra parte per aiutare a porre fine alla pandemia di Covid con un vaccino per adulti e bambini di tutte le età". KidCove è uno studio di espansione randomizzato, in cieco per l'osservatore, controllato con placebo, finalizzato a valutare la sicurezza, la tollerabilità, la reattogenicità e l'efficacia di due dosi da 50 µg di mRna-1273 somministrate a bambini sani a distanza di 28 giorni. La popolazione nello studio è suddivisa in tre gruppi di età (da 6 a meno di 12 anni, da 2 a meno di 6 anni e da 6 mesi a di 2 anni).
Il vaccino è stato "generalmente ben tollerato, con un profilo di sicurezza e tollerabilità generalmente coerente con lo studio Cove di fase 3 negli adolescenti e negli adulti. La maggior parte degli eventi avversi è stata di gravità lieve o moderata. Gli eventi avversi sollecitati più comuni sono stati affaticamento, cefalea, febbre e dolore al sito di iniezione", si legge nella nota.
I dati sulla sicurezza continuano ad accumularsi e lo studio continua ad essere monitorato da un comitato di monitoraggio della sicurezza indipendente. Tutti i partecipanti al trial saranno monitorati per 12 mesi dopo la seconda iniezione per valutare la protezione e la sicurezza a lungo termine. La raccolta dei dati continua. E la società prevede di inviare il materiale per la revisione paritaria e la pubblicazione in una rivista. Lo studio di fase 2/3 prosegue ad arruolare bambini di età compresa tra 6 mesi e meno di 6 anni.